一种增强mRNA-LNP组织靶向递送的方法
本发明属于生物,涉及一种增强mrna-lnp组织靶向递送的方法。
背景技术:
1、随着新冠病毒mrna疫苗的成功研发以及快速获批,mrna药物展现出其强有力的应用前景。通过设计信使核糖核酸(mrna)的序列理论上可以表达任何蛋白质,如抗原、治疗性蛋白、基因编辑元件等等,因此它可被用于预防性疫苗研制、蛋白替代疗法、基因编辑等诸多领域。此外,由于mrna生产工艺简单、成本低、周期短等特点,在临床转化中也备受青睐。但mrna携带负电荷且容易被酶降解,实际应用中依赖安全、高效递送载体,其中脂质纳米颗粒(lnp)被认为是最佳载体选择之一,临床在研的mrna药物项目超90%依赖于lnp。
2、lnp通常由可电离阳离子脂质、辅助磷脂、胆固醇和聚乙二醇脂质组成。其中,可电离阳离子脂质是实现mrna高效负载与溶酶体逃逸的关键,也是各科研单位和研发公司布局的重点。可电离阳离子脂质分子在低ph环境中(如ph 4.0)可以被质子化,进而结合mrna完成对其的包裹,而在生理环境中(ph 7.4)则不带电,使得lnp呈电中性。目前大多数的mrna-lnp可用于局部肌肉注射的疫苗应用,或静脉给药在肝脏分布和表达。然而,如何实现高效、特异的肝外器官靶向mrna递送是领域内的一个重要且关键问题,有望拓宽mrna的应用前景。
3、近年来,肝外器官靶向mrna递送也是取得了一些进展。主要有如下:1)电荷介导的靶向策略,通过在lnp中引入电正性阳离子脂质(如,季铵脂质dotap)可实现肺靶向mrna递送,引入电负性阴离子脂质(如,磷酸脂质18:1pa)可实现脾脏靶向mrna递送,被称为sortlnp技术(cheng等人,nat.nanotechnol.,15:313-320,2020);2)研发新型结构可电离阳离子脂质实现mrna靶向递送(如qiu等人,proc.natl.acad.sci.u.s.a.,119:e2116271119,2022);3)通过抗体修饰lnp策略,如在lnp表面修饰cd31抗体,成功实现mrna在肺部的表达(parhiz等人,j.control release,291:106-115,2018)。
4、上述方法均有一定的优势和不足,如正电性阳离子脂质的潜在毒性、新型结构可能的递送效率低、抗体修饰lnp特异性差等。新型的mrna-lnp药物具有非常广阔的应用前景,但是目前针对肝外器官、细胞的mrna靶向递送是难点。
技术实现思路
1、本发明解决的问题是提供增强mrna-lnp组织靶向递送的方法。
2、为了解决上述技术问题,本发明第一方面提供了一种增强核酸脂质纳米颗粒组织靶向递送性的方法,包括如下步骤:将具有组织靶向性的核酸脂质纳米颗粒表面修饰抗体,得到修饰抗体且具有组织靶向性的核酸脂质纳米颗粒,实现增强所述核酸脂质纳米颗粒的组织靶向递送性。
3、上文所述方法中,所述组织为肺、脑或脾。
4、或,所述抗体为靶向肺的抗体、靶向脑的抗体或靶向脾的抗体。
5、上文所述方法中,所述靶向肺的抗体为cd31抗体、plasmalemma vesicle-associated protein(pv1)抗体或cd326抗体。
6、或,所述靶向脑的抗体为转铁蛋白受体单克隆抗体(具体可以为如下任一种或几种组合:ox26、r17217和8d377)。
7、或,所述靶向脾的抗体为f4/80抗体,cd5抗体,cd4抗体,cd8抗体,cd3抗体或cd19抗体。
8、上文所述方法中,所述具有组织靶向性的核酸脂质纳米颗粒为电荷驱动靶向组织的核酸脂质纳米颗粒或非电荷驱动靶向组织的核酸脂质纳米颗粒;
9、所述电荷驱动靶向组织的核酸脂质纳米颗粒中脂质包括可电离阳离子脂质,马来酰亚胺修饰的聚乙二醇脂质和永久性阳离子脂质;
10、所述非电荷驱动靶向组织的核酸脂质纳米颗粒中脂质包括可电离阳离子脂质和马来酰亚胺修饰的聚乙二醇脂质。
11、上文所述方法中,所述电荷驱动靶向组织的核酸脂质纳米颗粒中脂质还包括辅助脂质;
12、所述非电荷驱动靶向组织的核酸脂质纳米颗粒中脂质还包括辅助脂质;
13、所述辅助脂质包括类固醇、磷脂和其他peg脂质中的任一种或任2种或3种。
14、上文所述方法中,所述永久性阳离子脂质(permanently cationic lipid)为具有季铵盐特性的脂质分子;
15、或,所述磷脂为具有药学上接受的双亲性脂质磷脂结构的脂质。
16、上文所述方法中,所述具有季铵盐特性的脂质分子为dotap、ddab、dotma或epc;
17、或,所述具有药学上接受的双亲性脂质磷脂结构的脂质为dope、dspe、pope、4me、dopc或dspc;
18、或,所述类固醇为胆固醇或其类似物;
19、或所述其他peg脂质为dmg-peg、dsg-peg或dspe-peg。
20、上文所述方法中,所述电荷驱动靶向组织的核酸脂质纳米颗粒为电荷驱动靶向肺的核酸脂质纳米颗粒;其中,各个脂质的摩尔比分别如下:所述可电离阳离子脂质占总脂质的摩尔比为20%-80%,所述永久性阳离子脂质占总脂质的摩尔比为10%-50%,所述马来酰亚胺修饰的聚乙二醇脂质占总脂质的摩尔比为0.5-5%,所述辅助脂质占总脂质的摩尔比为0-40%。
21、或,上文所述方法中,所述非电荷驱动靶向组织的核酸脂质纳米颗粒为非电荷驱动靶向肺的核酸脂质纳米颗粒,其中,各个脂质的摩尔比分别如下:所述可电离阳离子脂质占总脂质的摩尔比为20%-80%,所述马来酰亚胺修饰的聚乙二醇脂质占总脂质的摩尔比为0.5-5%,和,所述辅助脂质占总脂质的摩尔比为0-45%。
22、上述方法中,所述电荷驱动靶向肺的核酸脂质纳米颗粒中所述永久性阳离子脂质占总脂质的摩尔比为30%;
23、或,所述非电荷驱动靶向肺的核酸脂质纳米颗粒中所述可电离阳离子脂质占总脂质的摩尔比为50%。
24、上述电荷驱动靶向肺的核酸脂质纳米颗粒中可电离阳离子脂质可为sm-102、alc-0315、mc3、c12-200、ckk-e12、4a3-sc8或5a2-sc8,但不限于此;
25、上述非电荷驱动靶向肺的核酸脂质纳米颗粒中可电离阳离子脂质可为a3-n11f、306-n16b、113-n16b、98n12-5或7c1,但不限于此。
26、上述马来酰亚胺修饰的聚乙二醇脂质中的聚乙二醇脂质可为dspe-peg或dmg-peg,但不限于此。
27、上述胆固醇类似物可为β-sitosterol、7α-hydroxycholesterol或25-hydroxycholesterol,但不限于此。
28、上述dmg-peg可为dmg-peg2000,但不限于此。
29、上述dspe-peg可为dspe-peg2000,但不限于此。
30、上述dspe-peg-mal可为dspe-peg2000-mal,但不限于此。
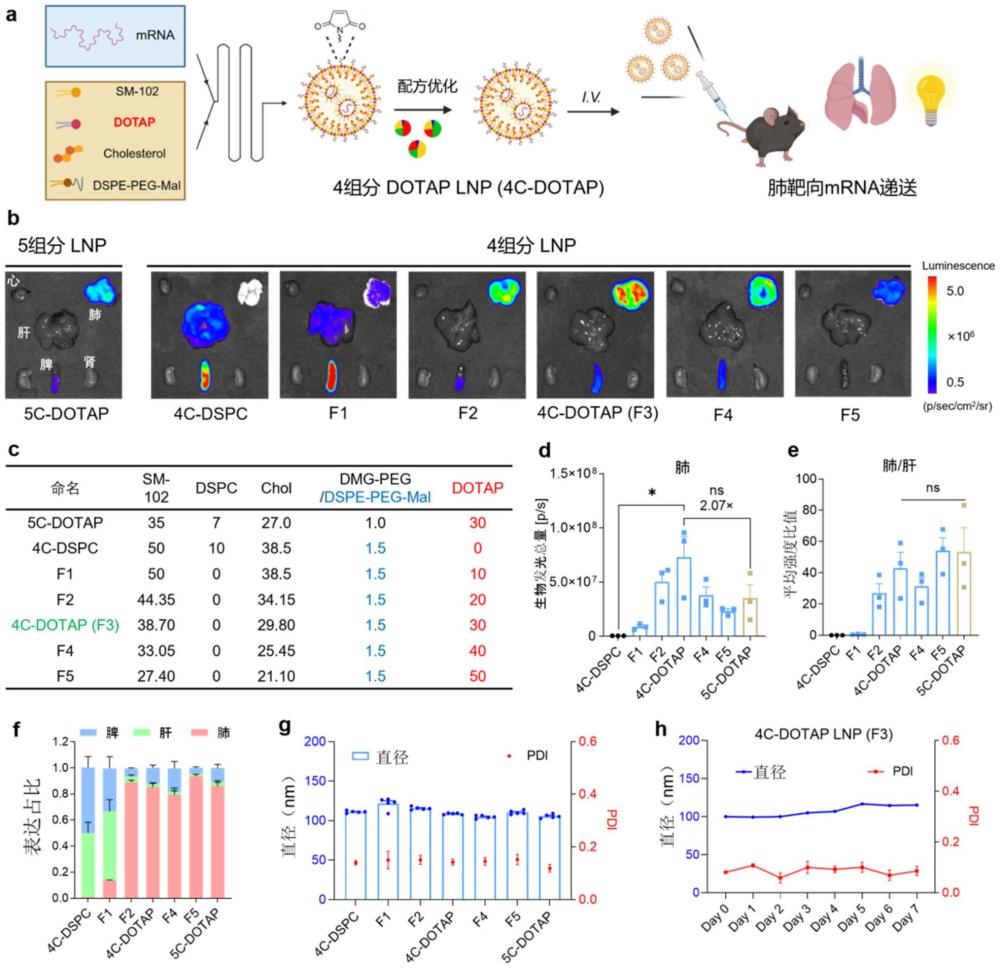
31、在本发明的一个实施例中,上述电荷驱动靶向肺的核酸脂质纳米颗粒由如下摩尔比的脂质组成:27%-50% sm-102、10-50% dotap、1.5%dspe-peg-mal和20-40% chol;总摩尔比不超过100%(具体如图1c)。
32、更进一步地,所述电荷驱动靶向肺的核酸脂质纳米颗粒由如下摩尔比的脂质组成:38.7% sm-102、30% dotap、1.5%dspe-peg-mal和29.8%胆固醇;总摩尔比不超过100%(具体为实施例中的4c-dotap lnp)。
33、在本发明的另一个实施例中,所述非电荷驱动靶向肺的核酸脂质纳米颗粒由如下摩尔比的脂质组成:23-50% a3-n11f、10-24% dope、1.5-5% dspe-peg-mal和38-48%胆固醇;总摩尔比不超过100%(具体如图7c)。
34、更进一步地,所述非电荷驱动靶向肺的核酸脂质纳米颗粒由如下摩尔比的脂质组成:50% a3-n11f、10% dope、1.5% dspe-peg-mal和38.5%胆固醇;总摩尔比不超过100%(a3-n11f lnp)。
35、上述核酸为经化学修饰或未经化学修饰的核酸分子。
36、上述经化学修饰或未经化学修饰的核酸分子例如dna分子或rna分子,优选地lnp中总脂质与核酸分子的质量比为约1-100:1。
37、上述经化学修饰或未经化学修饰的dna分子,可以是任何类型的dna分子(但不限于此),包括但不限于线性或环状dna、双链或单链或多链组装的dna、编码或非编码dna,其任选地选自质粒、寡脱氧核苷酸、基因组dna、dna探针、dna适配体、dna纳米框架、dna引物、同源修复dna模板、免疫刺激性dna或其组合。
38、上述经化学修饰或未经化学修饰的rna分子,可以是任何类型的rna分子(但不限于此),包括但不限于信使rna(mrna)、小干扰rna(sirna)、环状rna(circrna或orna)、向导rna(sgrna)、缺口向导rna(nicking sgrna)、小发夹rna(shrna)、病毒rna、复制子rna、转运rna(trna)、核糖体rna(rrna)、免疫刺激性rna(isrna)、微小rna(mirna)、小核rna(snrna)、rna适配体、反义rna、rna纳米框架、rna核糖核蛋白复合物或其组合。
39、进一步地,所述mrna表达具有治疗功能的蛋白、荧光报告的蛋白或杀伤肿瘤的蛋白。
40、上述抗体通过其表面的巯基基团与所述具有组织靶向性的核酸脂质纳米颗粒表面的马来酰亚胺基团连接得到。
41、上述修饰抗体且具有组织靶向性的核酸脂质纳米颗粒的递送效果高于所述具有组织靶向性的核酸脂质纳米颗粒。
42、第二方面,本发明提供了由第一方面所述方法制备的修饰抗体且具有组织靶向性的核酸脂质纳米颗粒。
43、或,本发明提供了所述修饰抗体且具有组织靶向性的核酸脂质纳米颗粒在制备靶向组织产品中的应用。
44、或本发明提供了一种制备所述修饰抗体且具有组织靶向性的核酸脂质纳米颗粒的方法,包括第一方面所述步骤。
45、上述制备修饰抗体且具有组织靶向性的核酸脂质纳米颗粒的方法,具体包括如下步骤:
46、a1)将所述具有组织靶向性的核酸脂质纳米颗粒中各个脂质溶于有机溶剂中,得到脂质有机相;再与mrna水相进行混合,得到具有组织靶向性的核酸脂质纳米颗粒;
47、a2)将所述具有组织靶向性的核酸脂质纳米颗粒修饰所述抗体,得到修饰抗体且具有组织靶向性的核酸脂质纳米颗粒。
48、或本发明提供了一种靶向组织产品,其活性成分为所述修饰抗体且具有组织靶向性的核酸脂质纳米颗粒。
49、上述产品为靶向递送平台或药物。
50、上述组织为肺、脑或脾。
51、基于上述背景,本发明提出:结合上述多种策略有望弥补当前靶向mrna-lnp面临的不足。因此做了如下实验:1)参考sort lnp技术,通过引入带电荷脂质获得靶向lnp,与5组分sort lnp不同,靶向lnp维持4组分,并将lnp中的peg-dmg脂质进行全替换为dspe-peg-mal(该脂质可以提供用于抗体修饰的活性基团);2)运用cd31抗体建立对lnp表面修饰技术,并获得抗体与lnp的最佳比例;3)分别在电荷驱动的肺靶向lnp、结构驱动的肺靶向lnp中,运用cd31抗体修饰均显著提升了mrna-lnp的递送特异性、安全性、有效性。4)运用上述增强型靶向lnp,完成了白介15超级激动剂mrna的肺靶向递送,在肺部肿瘤转移小鼠模型中介导了高效率肿瘤免疫治疗。这种新型的、抗体增强型肺靶向mrna-lnp递送策略可以为肺部疾病的治疗带来新的突破,并极大程度拓宽mrna-lnp药物的应用深度和广度。
52、本研究中,综合领域内靶向lnp的研发策略,以期通过“双重靶向”手段提升mrna-lnp递送的各项性能。主要的创新点和关键点如下:
53、1)参考sort lnp技术(通过额外添加阳离子脂质到4组分lnp中实现肺靶向递送),优化改进基于dotap正电荷的肺靶向lnp处方,使用正电荷脂质dotap完全替换掉lnp中辅助磷脂dspc,并使用dspe-peg-mal完全替换dmg-peg。与sort lnp不同,不仅保留4组分,同时用dspe-peg-mal全替换原有dmg-peg,为后续抗体修饰lnp提供了mal的活性基团。其中,含有30% dotap的lnp处方(命名为4c-dotap lnp)具有最佳的转染效果和较好的特异性,效果优于先前报道的5组分sort lnp(5c-dotap lnp))。
54、2)建立最佳cd31抗体与lnp比例。通过优化cd31抗体用量,实现高效的基于抗体修饰的肺靶向mrna递送(命名为anti lnp)。
55、3)通过在4c-dotap lnp上修饰cd31抗体的协同靶向策略(命名为synergistictargeted lnp,syntar lnp),使得肺靶向mrna递送效率进一步显著提高。syntar lnp可以高效转染、编辑肺脏内皮细胞、上皮细胞以及免疫细胞,并且稳定性好。
56、4)通过与其他肺靶向lnp策略进行对比,syntar lnp相比于anti lnp具有更优越的特异性,显著降低了肝脏部位的脱靶表达。syntar lnp相较于4c-dotap lnp和anti lnp具有更高的肺部递送效率,以及相较5组分sort lnp更好的安全性。
57、5)前期建立的结构驱动靶向lnp技术(简称star lnp,专利申请号pct/cn2023/137998)中,可电离阳离子脂质a3-n11f lnp具有肺靶向递送mrna功能。利用上述syntar策略,在a3-n11f lnp上修饰cd31抗体进一步增强了递送效率,验证这种结合策略的普适性。
58、6)最后,基于早先开发的白介素15超级激动剂mrna技术(专利申请号pct/cn2024/084406),运用syntar lnp体系介导高效il-15mrna肺靶向递送,并实现了小鼠肺部肿瘤转移的高效抑制,证明了syntar lnp平台的有效性以及疾病治疗应用的能力。
59、7)基于1-6,开发出一种广谱、通用且递送效率和特异性更好的mrna-lnp肺脏靶向递送技术,并且能够高效特异转染肺部的内皮细胞、上皮细胞和免疫细胞,为肺部疾病的治疗提供了全新的治疗手段。并且有合理的理由推断,通过抗体联合靶向lnp的“双重靶向”策略有望扩展到肺部之外的mrna递送和治疗中,如脑、肝、肾脏、心脏等。
60、本发明通过在新型肺靶向lnp的基础上结合抗体修饰策略(双重靶向),成功实现了更加高效、特异、安全的肺脏靶向mrna递送。且该策略适用于任何种类的靶向lnp中(本项目中有电荷驱动的dotap lnp和结构驱动的star lnp两种)。最后通过这种新型的lnp平台递送治疗性的il-15超级激动剂mrna,实现了对于肺部肿瘤的有效抑制。该成果对于遗传性肺脏疾病,肺损伤,肺特发性纤维化,囊性纤维化,肺癌等疾病的治疗具有重要参考意义和价值。此外,有理由相信,只要选择合适的抗体以及靶向lnp,该策略可扩宽到肺部之外的器官靶向递送和治疗当中,如脑、心脏、肾脏、胰腺等。
技术研发人员:程强,宗岩
技术所有人:北京大学
备 注:该技术已申请专利,仅供学习研究,如用于商业用途,请联系技术所有人。
声 明 :此信息收集于网络,如果你是此专利的发明人不想本网站收录此信息请联系我们,我们会在第一时间删除
