一种人参皂苷Rg3载药系统及其制备方法和应用
本发明属于人参皂苷rg3药物制备,特别涉及一种人参皂苷rg3载药系统及其制备方法和应用。
背景技术:
1、结直肠癌(colorectal cancer,crc)是常见的消化道恶性肿瘤,是多种致病因素(如基因、饮食和环境)综合作用下形成的结直肠黏膜上皮和腺体部分发生的恶性肿瘤,在全球癌症发病率高,严重危害生命健康,其早期诊断率较低,大多数患者确诊时已是中晚期,部分已出现发生转移。
2、人参皂苷rg3(ginsenoside rg3,g-rg3)是从人参中提取的四环三萜皂苷,是抗癌新药“参一胶囊”的主要成分,本身具有良好的抗癌活性。g-rg3既可通过调控tme、提高机体免疫力以“扶正”,也可直接作用于肿瘤细胞发挥抑制增殖迁移、促凋亡作用以“解毒”,实现crc的多靶点多环节治疗。g-rg3作为人参中的四环三萜皂苷成分,其水溶性差、脂溶性弱、半衰期短,在壳核结构中的自组装的能力较难,口服后进入胃肠道内的被其中的酶或肠道细菌所代谢,且存在首过效应而血药浓度低,生物利用度仅为2.63%,因而大大限制了临床应用。
3、口服结肠靶向给药系统(oral colon-specific drug delivery system,ocdds)可使药物不在上消化道释放,而在回盲部或结肠释放,发挥局部或全身的治疗作用,常用于结肠部位疾病的治疗,如溃疡性结肠炎和结肠癌等,即有利于药物在病变部分蓄积,提高生物利用度,又能提高患者顺应性。
4、白及多糖(bletilla striata polysaccharides,bsps)是从兰科植物中药白及bletilla striata(thunb.)reichb.f干燥块茎中提取的一种水溶性多糖。bsps易溶于热水,微溶于冷水,不溶于乙醇。其单糖组成较为一致,大多是由甘露糖(mannose,man)和葡萄糖(glucose,glc)经1→4糖苷键键合而成两者,比例集中在4:1-2:1,分子量分布在1.0×104~1.0×105da之间。bsps本身具有止血、促进伤口愈合、保护消化道黏膜、抗炎、抗氧化、抗肿瘤和调节免疫等多种药理活。作为一种天然高分子材料,bsps具有结构稳定、生物可降解、生物安全性高等特点,常被广泛用于医药原料和药用辅料,发挥“药辅合一”作用。由于bsps主链上含有大量活性羟基,易于结构改造,采用不同的设计策略对其结构母体进行修饰,可获得具有不同功能的载体材料。
5、bsps为亲水性高分子材料,通过引入疏水基团,如胆甾醇琥珀酸酯等可制备两亲性纳米载体,在水相中能够通过自组装形成具有核壳结构的纳米胶束体系,其疏水内核有利于包载难溶性抗肿瘤药物,提高药物生物利用度,并通过高渗透长滞留效应(enhancedpermeability and retention effect,epr)被动靶向肿瘤组织。
技术实现思路
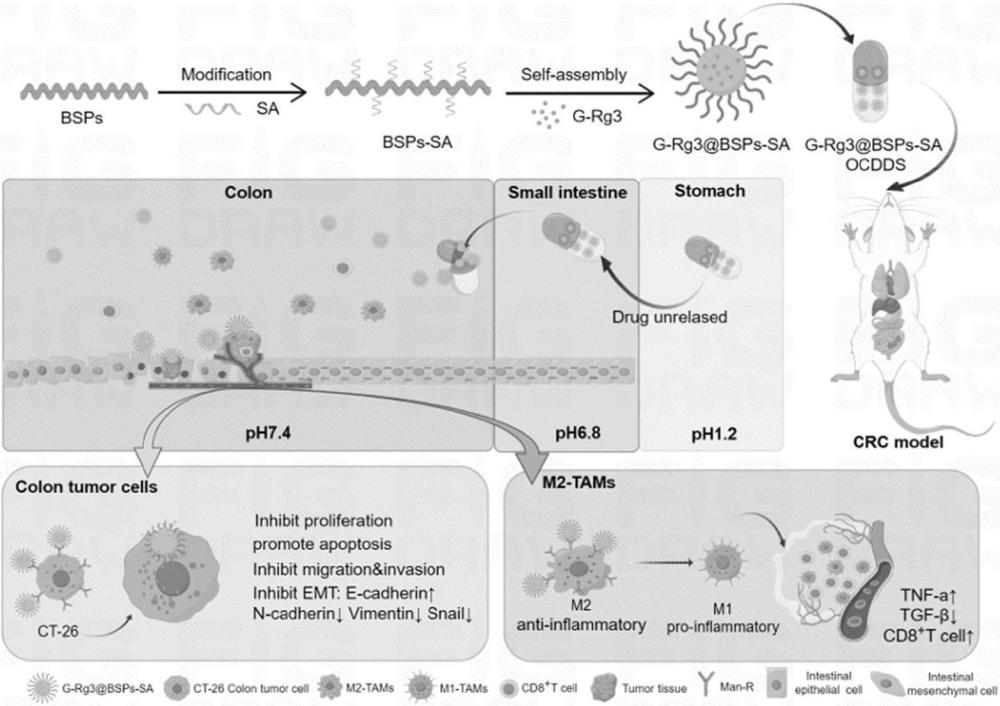
1、本发明的目的在于,提供一种g-rg3@bsps-sa结肠溶胶囊及其制备方法。本发明制备的g-rg3@bsps-sa结肠溶胶囊,可以在结肠特定ph环境中降解,释放出g-rg3@bsps-sa聚合物胶束。bsps中大量暴露man分子分别与结肠癌细胞和m2-tams上高表达的man-r结合,以主动靶向的方式促进细胞摄取,在细胞内溶酶体环境中(ph5.0)释放药物,分别发挥其“扶正解毒”双重功效,提高了药物在结肠中的可利用度,发挥抗肿瘤作用,如图1所示。
2、人参皂苷rg3是具有“扶正解毒”功效的药物,由于其脂溶性弱,在壳核结构中的自组装的能力较难,因此本发明采用了乳化溶剂挥发法对制备工艺进行了改进。本发明采用乳化溶剂挥发法制备g-rg3@bsps-sa聚合胶束,并对其体外释药行为进行评价。将其装入结肠溶胶囊壳中,制备g-rg3@bsps-sa ocdds,并对其释药行为和初步稳定性进行考察。通过对肿瘤细胞和m2-tams的双靶向功能,实现对结肠癌“抑制肿瘤细胞生长、调控免疫微环境”的多环节调控作用,进而有效抑制结肠癌发生发展。
3、为了实现上述任务,本发明是通过以下技术方案得以实现:
4、一种g-rg3@bsps-sa结肠溶胶囊,其特征在于,由下述组分组成:人参皂苷rg3原料药、两亲性白及多糖聚合物载体、结肠溶胶囊壳。
5、两亲性白及多糖聚合物载体包括以下两种化合物:
6、(a)、白及多糖(bsps),亲水性高分子材料。
7、(b)、硬脂酸(sa),疏水基团。
8、上述g-rg3@bsps-sa结肠溶胶囊,采用水提醇沉法从中药白及中提取bsps,通过脱脂脱色、savag脱蛋白等步骤精制,得到白及粗多糖,经deae-52和sephadexg-200纯化得bsps。采用n(sa):n(dmap):n(edc)=1:1:1.2比例进行合成bsps-sa聚合物。
9、上述g-rg3@bsps-sa聚合物纳米胶束,采用透析法制备bsps-sa聚合物胶束,经自组装得到澄清透明的高分子溶液,经tem观察胶束呈球形,且分布较为均匀;经malvern粒径分析仪测定粒径为145.12±8.54nm,pdi为0.18±0.012(pdi<0.3),ζ电位为-23.3±0.031mv;7天内纳米胶束的粒径、分散指数和ζ电位无显著性差异(p>0.05),bsps-sa聚合物纳米胶束稳定性良好,可用于后续载药。
10、上述g-rg3@bsps-sa聚合物纳米胶束,采用乳化溶剂挥发法制备后,其呈圆球形,粒径为185.43±1.34nm,pdi为0.21±0.01,ζ电位为-19.2±0.32mv,载药量为9.54±0.24%%,包封率为83.90±2.20%。在3种不同介质中(ph7.4、ph6.5、ph5.0)的48小时累积释放度分别是65.32±3.22%、79.56±4.28%、85.24±3.42%,释药速度明显大于游离g-rg3药物,在正常结肠液中较为稳定,在肿瘤酸性微环境下加速释放,入胞后有利于在溶酶体酸性环境下快速释药。
11、上述g-rg3@bsps-sa结肠溶胶囊在胃和小肠中均不释药,在模拟结肠液中48h药物累计释放量为63.54±3.12%,能够提高药物在结肠部位的蓄积。
12、上述g-rg3@bsps-sa聚合物纳米胶束,以coumarin-6作为荧光探针,采用荧光显微镜观察细胞摄取作用,coumarin-6@bsps-sa聚合物胶束经甘露糖受体介导入胞,ct-26细胞和m2-tams摄取率分别为游离coumarin-6的1.79倍、1.46倍。
13、上述g-rg3@bsps-sa聚合物纳米胶束中的bsps-sa载体,采用cck-8测定细胞毒性结果表明,bsps-sa载体对ct-26细胞和m2-tams的细胞活力均无明显影响,具有良好的生物安全性。。
14、上述g-rg3@bsps-sa结肠溶胶囊是指用于口服的双向结肠靶向药物。
15、上述g-rg3@bsps-sa结肠溶胶囊的制备方法,其特征在于,按以下步骤进行:
16、(a)、bsps的提取:
17、将白及饮片放入60℃烘箱中充分干燥,粉碎过80目筛。取100g白及粗粉,加入20倍量的蒸馏水,90℃水浴锅中提取5小时,过滤,取残渣,重复提取3次。用尼龙纱布过滤,收集合并滤液,经旋转蒸发浓缩至原体积的1/3,加入3倍体积的无水乙醇,静置过夜以充分沉淀。收集沉淀,真空干燥,得到白及多糖提取物。
18、取适量白及多糖提取物,加入10倍体积石油醚,70℃条件下回流提取4h,过滤,取残渣。加入10倍量的80%乙醇,回流提取4h,过滤收集残渣。
19、在脱脂脱色后的多糖水溶液中,加入木瓜蛋白酶(0.5mg/ml),用naoh溶液(1m)调节ph至7.0,置于50℃水浴中酶解2h,放入沸水浴灭酶10min,冷却至室温。采用sevag法除蛋白,将多糖溶液加至分液漏斗中,加入20%sevag试剂(三氯甲烷与正丁醇体积比为5:1)剧烈振摇20min,静置4h,弃去分层交界处的变性蛋白,重复操作不少于3次,直至分层交界处无明显浑浊为止。收集上层溶液,旋转蒸发浓缩至原体积的1/3,加入3倍体积的无水乙醇,静置过夜以充分,收集沉淀,干燥后得到白及粗多糖(crude bletilla striatapolysaccharides,c-bsps)。
20、(b)、bsps的纯化:
21、称取200mg c-bsps,溶解于20ml去离子水中。用胶头滴管缓缓将白及多糖水溶液滴入deae-52纤维素柱(4cm×60cm)开展层析。依次用去离子水和0.1、0.2、0.5mol/l nacl溶液进行梯度洗脱,流速为1ml/min,每5ml收集于1个试管中。
22、称取100mg经deae-52柱层析纯化后的白及粗多糖,溶于10ml去离子水,通过sephadexg-200葡聚糖凝胶柱(2.3cm×90cm)进行层析。用0.02mol/l的nacl水溶液层进行洗脱,流速为15ml/min,每5ml收集于1个试管中。
23、(c)、bsps-sa的制备:
24、分别称取142.24mg sa,61.08mg 4-二甲氨基吡啶(4-dimethylaminopyridine,dmap)和93.14mg 1-乙基-3-(3-二甲基氨基丙基)碳二亚胺(1-ethyl-3-(3-dimethylaminopropyl)carbodiimide,edc)溶解于3ml dmso中,室温下磁力搅拌活化2h,得到活化反应液。称取400mg bsps溶于4ml dmso,逐滴加入到活化反应液中,于75℃反应4h,再于室温下反应24h。反应结束后将上述反应物装入透析袋(3500da)透析24h,除去dmso,用等体积的乙酸乙酯重复萃取3次,以除去未反应的sa,40℃旋转蒸发以除去乙酸乙酯,将产物冷冻干燥,得到bsps-sa。
25、(d)、bsps-sa聚合物胶束的制备:
26、采用透析法制备bsps-sa聚合物胶束。精密称取25.0mg bsps-sa,加入5ml dmso完全溶解后,全部转移至透析袋中(8000da),将透析袋置于500ml纯水中室温透析,每8h换一次水,累计透析48h,过0.45μm微孔滤膜,转移定容至25ml容量瓶中,得到空白聚合物胶束溶液。
27、(e)、g-rg3@bsps-sa聚合物纳米胶束的制备:
28、精密称取25mg的bsps-sa,加入4mldmso完全溶解后,全部转移至透析袋中(8-14kda),将透析袋置于500ml纯水中室温透析,每8h换一次水,累计透析48h,过0.45μm微孔滤膜,转移定容至25ml容量瓶中,得到1mg/ml空白胶束溶液。精密称取5mg的g-rg3溶解于2.5ml甲醇中,得到2mg/ml g-rg3溶液。取1.6ml g-rg3溶液,以250rpm转速下逐滴滴入空白bsps-sa胶束中,室温下搅拌4h,挥去甲醇,过0.45um微孔滤膜,冷冻干燥,即得g-rg3@bsps-sa聚合物胶束冻干粉。
29、(f)、g-rg3@bsps-sa结肠溶胶囊的制备:
30、称取g-rg3@bsps-sa聚合物纳米胶束冻干粉适量,直接灌装于小鼠专用结肠溶胶囊(黄山胶囊有限公司提供)中,灌装后在囊帽与囊体接口处涂上胶液,晾干,即得。每粒胶囊中聚合物胶束粉末的装量为4mg,含g-rg3约为0.4mg。
31、本发明的有益之处在于:
32、本发明公开了一种人参皂苷rg3结肠溶胶囊及其制备方法,制备得到的g-rg3@bsps-sa结肠溶胶囊是一种口服双向结肠靶向制剂,人参皂苷rg3@bsps-sa ocdds可以经甘露糖受体介导,靶向m2-tams促进向m1型重编程,减少tgf-β、提高tnf-α,诱导cd8+t细胞浸润,逆转免疫抑制环境,重构肿瘤微环境以“扶正”;靶向结肠癌细胞抑制细胞增殖、迁移和侵袭,促进细胞凋亡,下调snail核转录因子的表达抑制上皮间质转化,抑制肿瘤生长而“解毒”,有效控制结肠癌发生发展。
技术研发人员:胡容峰,高松,方文悠,方灿灿,徐明超,孙凌峰,王楠
技术所有人:安徽中医药大学
备 注:该技术已申请专利,仅供学习研究,如用于商业用途,请联系技术所有人。
声 明 :此信息收集于网络,如果你是此专利的发明人不想本网站收录此信息请联系我们,我们会在第一时间删除
